東和薬品の品質と
安全性の取り組みについて

東和薬品は、ジェネリック医薬品の
確かな品質と安全性の確保に、
徹底的に取り組んでいます。
東和薬品の品質方針
東和薬品グループは、優れた製品と
サービスを創造することによって、
人々
の健康に貢献することをお約束します。
- 常に患者さんを第一に考え、必要とされる確かな品質の医薬品及び情報を提供します。
- 最新の国際標準に適合する品質保証体制を構築し、関連法律と規制要求事項を遵守し、適切な製造管理と
品質管理を実践します。 - 製造現場から経営トップまで、全ての社員が一体となって、品質優先の価値観を浸透させていきます。
- 最新の技術で改良、改善を重ね、高品質な医薬品を安定的に供給いたします。
- 最新の科学的知見に基づくプロアクティブな取り組み及び積み上げてきた知識管理を基に、
常に継続的改善を実施します。
より高いレベルで東和薬品の医薬品
をお届けするために。
医薬品の製造には、GMP(*)と呼ばれる、国が定めた「医薬品の製造管理及び品質管理の基準」が基本にあります。
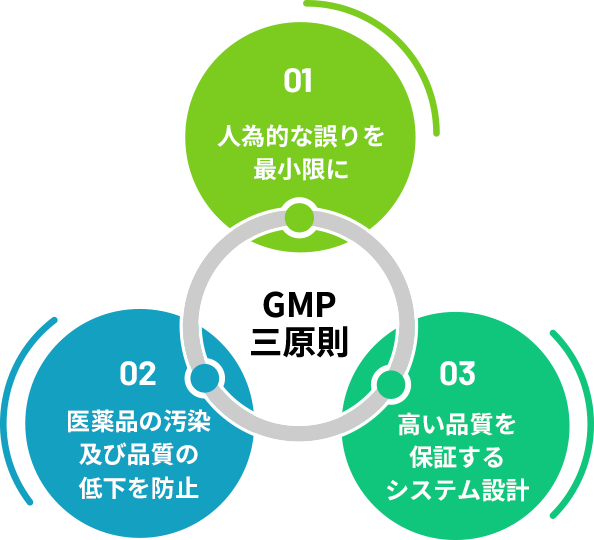
GMPには三つの原則があり
「①人為的な誤りを最小限にすること」
「②医薬品の汚染及び品質の低下を防止すること」
「③高い品質を保証するシステムを設計すること」
が定められています。

東和薬品は、山形、大阪、岡山の全ての工場においてGMP三原則を遵守した手順を設定。社員には継続して教育訓練を行い、一人一人が医薬品製造に携わる者としての高い意識を持って業務にあたるよう、日々取り組んでいます。さらに、より厳しいルールの中で正しいものを作り出すために、国際的基準であるPIC/S GMPやICHガイドラインも積極的に取り入れ、人為的な誤りをより排除できる体制をつくっています。
医薬品は命に関わるものですが、外から見ても、その品質がどのようなものかはわかりません。だからこそ、品質や安全性に向き合うことが重要です。私たちはGMPを遵守し承認書の記載内容に則り、誰でも、同じレベルの医薬品をつくることができるようにする必要があると考えます。東和薬品は、常に、より高いレベルで必要とされる、確かな品質の医薬品を生み出すことに努めています。
* GMP(Good Manufacturing Practice)医薬品製造における厳しい製造管理、品質管理に関する基準のこと。
人為的な誤りを
最小限にするための取り組み
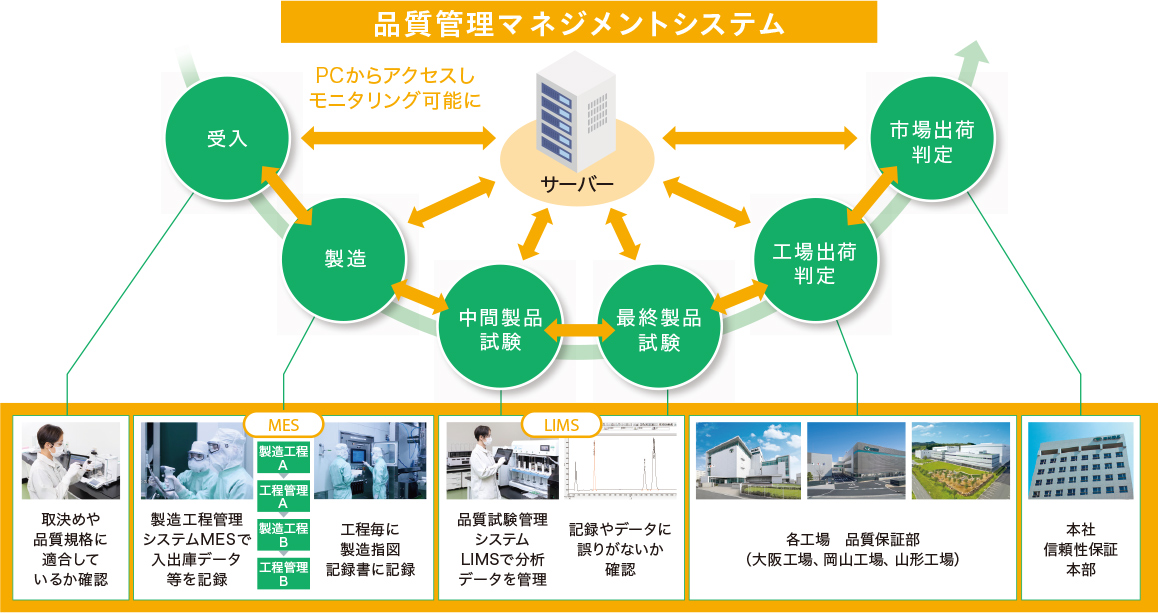
東和薬品では、GMP三原則のひとつ「人為的な誤りを最小限にすること」の取り組みとして2つのシステムを導入しています。
-

製造実行管理システム
MES(Manufacturing Execution System)製造工程の把握や管理、
作業者への指示、支援などを行うシステム。 -

医薬品の品質試験を統括管理するシステム
LIMS( Laboratory Information Management System)ネットワークを介して、分析結果が分析機器から
直接システムに入力される試験業務を統合管理したシステム。
このシステムと並行して、人によるダブルチェックを実施することで、人為的な誤りをより排除できる体制を構築しています。多くの品目の医薬品を製造するジェネリック医薬品メーカーである私たちには、MESやLIMSというシステムと人によってしっかりと管理することで、さまざまな製造工程ごとのきめ細やかなチェックを機能させています。
製造現場から経営トップまで。
意識を一つにした連携体制。
品質に関する情報共有の仕組み
定期的な情報共有で現場から経営幹部まで遅滞なく連携
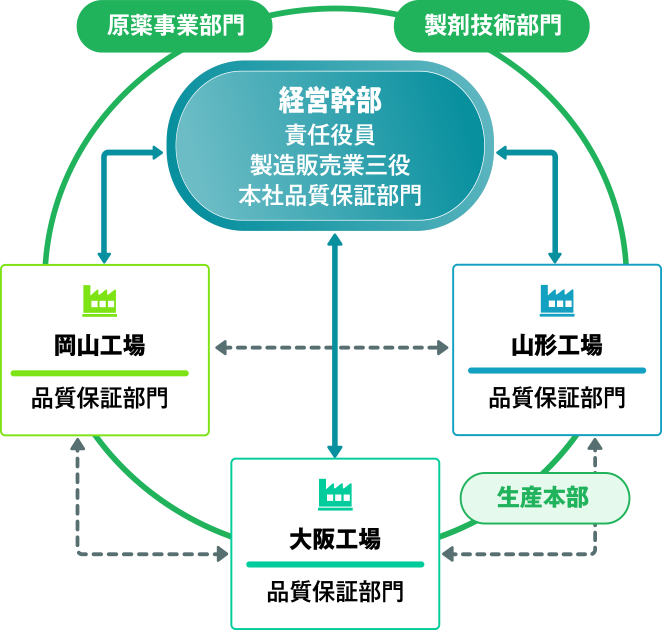
現在、私たちは、約700品目の医薬品を製造しています。その全ての医薬品を、徹底した品質管理のもとでお届けするために、本社の品質保証部門を中心に、工場の監査も定期的に実施。
また、品質管理への意識向上と絶え間ない改善のために、本社と3つの工場で品質に関する情報共有や事例研究を行っています。
さらに、その定例報告会に経営幹部も参画し、現場から経営幹部まで遅滞なく情報が共有される仕組みを構築することで、医薬品の適切な品質と安全性の確保に取り組んでいます。
教育訓練と独自の認定制度で、
高い意識を持つ人財を育成しています。
GMPで定められている「人為的な誤りを最小限にすること」。
私たちは、この意味を正しく理解し、医薬品製造に携わる社員の育成に取り組んでいます。
■ 人為的な誤りを起こさないための
システム導入と教育訓練
前述の製造工程や品質試験において、人為的な誤りを最小限に抑えることを目的にしたMES・LIMSといったシステムに加え、製造時に遵守すべき承認書の記載内容と、その背景にある薬事的要求事項を記載したマニュアルを作成し、承認書通りに製造することの重要性を銘じさせる教育訓練を実施しています。

■ 社内独自の認定制度
(エキスパート)の実施
通常の教育訓練に加え、製造・包装・試験・品質保証といった各部門で、より高い技術や知識を持つ者を「エキスパート」として認定する独自の制度を導入。各分野におけるスペシャリストが製造管理、品質管理を行える仕組みにするとともに、自らが品質確保に対する高い意識を持った社員の育成を推進しています。